生物可降解依維莫司洗脫聚乳酸支架在復雜冠脈中的運用-澳門經驗
鄧錫偉 劉書雷
澳門鏡湖醫院
冠脈介入治療技術發展迅速,從最初的PTCA,到BMS、DES支架,已經發展到目前的生物可吸收支架(BVS)。目前的ABSORB BVS支架骨架部分為聚L-乳酸、由聚DL乳酸包被,兩種組分均天然可吸收、代謝完全,其中骨架部分約2年內可完全再吸收.藥物塗層依維莫司和XIENCE V支架的藥物密度和釋放速率類似, 通過XIENCE系統進行輸送.支架的塗層為非晶體結構,厚度為2-4um,由依維莫司/聚DL乳酸按照比例為1:1組成的控釋系統.骨架部分為高密度晶體結構,可以保證系統的完整性和足夠的徑向支撐力.
BVS支架的目的在於提供暫時的血管支撐,使得血管生理性的修復可以自然進行. BVS支架釋放後,隨著時間的推移,其功能呈現出週期性變化,整體上可以分為3個期(血運重建期、血管功能恢復期和支架再吸收期)(Fig 1). 血小板聚集、白細胞粘附性炎症反應、血管平滑肌細胞增殖和遷移、基質沉積等不良事件主要集中在前1-3個月的血運重建期, 依維莫司主要在前1個月釋放,3個月左右釋放完畢,同時內皮化過程隨著依維莫司釋放減少逐漸加速,3-6個月可以良好內皮化,同時隨著支架的逐步吸收,其徑向支撐從3個多月開始逐步下降, 半年左右徑向支撐明顯減弱,此時血管基本完成重建過程,逐步進入到支架吸收期[1, 2].
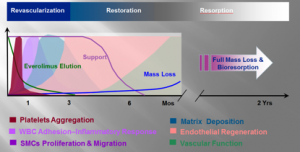
Fig1 BVS支架功能的周期性
BVS支架較BMS支架和DES支架的優勢在於可以減少雙聯抗血小板治療的時間,良好控制內膜的增厚,可以恢復血管的舒縮運動和擁有良好的生物相容性[3]。 BVS支架的有良好的生物相容性,針對支架的炎症反應輕微.根據雅培公司的研究數據,較傳統的Cypher支架,BVS炎症反應低,1年之後,炎症反應基本可以忽略不計。同時較傳統支架,植入後的異物反應輕,2年後BVS支架完全吸收,異物反應可以完全消失。
總體而言,BVS支架的優勢在於:1)可以恢復血管的舒縮功能;2)有利於血管的重塑和後期管腔擴大優勢;3)側枝受累少;5)生物相容性高;6 )邊緣血管反應;7)消除支架貼壁不良。其中邊緣血管反應為醫源性的、器械相關的,生物因素綜合效應。
目前研究提示[4-6],在下面的人群中,可以推薦使用BVS支架:1)年輕患者,有潛在的干預後可以恢復到更自然狀態的血管,沒有永久性金屬支架約束血管,可以對一些生理需求作出反應,例如有需要減少抗血小板治療的時間,對有更多獲益的自然功能血管的要求高。 2)未來需要干預的年輕患者,植入永久金屬支架複雜或者被迫採用金屬支架:無論是PCI還是CABG,不採用永久支架植入可為未來的介入治療提供更多選擇。存在金屬支架會增加CABG的難度。多層CT掃描(MSCT)可能幫助通過非侵入性的方法制定再治療策略。
目前已經有9個臨床研究,對BVS支架的臨床使用效果進行了評價,其中ABSORB Cohort A研究已於2011年完成,ABSORB Cohort B研究到2013年已經跟踪隨訪3年,ABSORB Extend 和ABSORB Physiology研究已經跟踪隨訪近1年,其他5個研究目前仍在招募和跟踪隨訪中,截止到2013年,總計有8400名患者納入研究。中國地區的ABSORB China BVS研究也從2013年開始起步,而且隨著臨床研究的推進,BVS支架的設計也得到提高:支架骨架的分佈更加統一,血管壁的支持更加均衡,足夠的徑向支撐,支架面積丟失更低,室溫下保存,在輸送系統中的操控性得到提高。但支架骨架和塗層的材料,骨架厚度,藥物釋放速度及支架完全吸收時間保持一致。
其中於2011年完成的ABSORB Cohort A研究,納入了30名患者,跟隨隨訪期為5年,在歐洲和新西蘭的的4個單位完成,納入的患者均為男性,單組研究,主要目的在於評估支架的安全性和效果,研究終點為需要PCI干預的臨床和影像事件,干預血管為參考血管直徑大於3mm,單一新發冠脈病變。通過MSCT,IVUS,OCT和血管舒縮功能檢查進行跟踪隨訪。 IVUS檢查支架植入後即刻、6個月、2年和5年的平均管腔面積、斑塊面積和血管面積,提示BVS支架有顯著的後期管腔擴大獲益,後期斑塊面積明顯縮小,血管基質沉積減少,血管面積明顯減少。 MSCT得到的結果與IVUS類似。其中OCT 2年跟踪結果顯示,支架植入即刻,邊支開口部位的BVS支架沒有完全貼壁,6個月的時候,可以看到部分支架貼壁不良持續存在、部位已經消失,2年的時候,橫斷面上可見幾乎完整的、光滑內皮輪廓。最後仍有高反射提示可能存在骨架,但支架骨架完全吸收。提示BVS支架可以明顯減少對邊支的影響。部分病例,OCT提示植入後支架完全貼壁,6個月時可見遲髮型貼壁不良,管腔內緣褶皺,2年後,平滑的內皮輪廓幾乎環繞整個橫斷面,最終儘管仍有高反射提示可能存在骨架,但支架完全吸收,提示BVS支架可以有效消除貼壁不良現象。 ABSORB Cohort 研究跟踪2年時評價了血管的舒縮功能,分別利用乙酰膽鹼擴張血管和甲基麥角鹼收縮血管,發現血管的舒縮功能恢復,對血管活性物質的生理反應重新出現[8],提示BVS支架可以有效恢復血管的舒縮功能。 ABSORB Cohort A 5年隨訪研究提示BVS支架長期預後非常理想,6個月至5年支架沒有新發的主要心血管不良事件(MACE),5年內沒有支架內血栓的形成。
隨後的ABSORB Cohort B和Extend研究目前已經跟踪隨訪3年,單組研究或與XIENCE V DES支架的比較,初步結果均提示BVS支架優勢明顯,早期的幾項研究均為非隨機對照試驗,BVS支架的遠期療效還有待進一步的跟踪隨訪和大規模臨床隨機對照試驗的驗證。
關於BVS支架的選擇,首先通過QCA(冠脈造影定量分析)分析病變近端和遠端參考血管的最大管腔直徑(Dmax),對參考血管的直徑存有疑慮、有粥樣硬化斑塊或鈣化病變時還可以通過IVUS或OCT幫助明確診斷。目前Dmax在2-3mm,2.5-3.3mm和3.0-3.8mm之間時,分別推薦選擇的BVS支架直徑分別為2.5,3.0和3.5mm。支架至少騎跨狹窄部位前後各2mm,同一病變放置2個支架時,銜接部位的長度推薦為1-4mm。預擴張病變時,預擴張球囊的直徑應比支架小0.5mm,首次預擴張無效或固定殘餘狹窄>40%而採用非順應性球囊時,推薦與支架直徑一致。選用最小管徑為1.8mm的6F或更大內腔的指引導管,保持同軸,在鉑金Marker的指示下送至合適部位,不推薦BVS支架用於迂曲病變或顯著鈣化病變。支架釋放時,球囊膨脹時間至少30s,推薦逐步膨脹法,每5s增加壓力2atm,不應超過額定爆破壓。支架植入部位的血管直徑對比造影時看上去可能偏小,後擴張只推薦在有明顯殘餘狹窄後支架成角時使用。後擴張球囊應該選用高、低順應性球囊。直徑2.5,3.0和3.5mm的BVS支架,推薦的後擴張球囊分別為2.75-3.0mm,3.25-3.5mm和3.75-4.0mm。支架植入後,雙聯抗血小板治療時間根據臨床情況,推薦至少半年或者更長時間。
BVS支架不僅適用於簡單病變。對於一些複雜病變,初期研究的結果也很好。 Diletti R等[9]研究了在直徑<2.5mm的小血管中使用BVS支架的效果,結果顯示在小血管中使用3.0mm的支架安全、有效,和在大血管中使用BVS支架相比,臨床情況和血管造影結果類似;Fernández 等研究了BVS支架在LM中的使用情況[10],該例患者56歲,男性,NSTEMI,既往曾接受過冠脈搭橋,有高血壓、糖尿病病史,作者發現3.5mm的BVS支架16atm壓力下直徑可以達到4mm,邊支血管開口沒有病變的情況下,證實了BVS支架在分叉病變處的可行性;對於分叉病變,Gogas BD[11]和Van[12 ]各有一例報導,均在手術即刻取得良好效果。
BVS支架在澳門鏡湖醫院運用已有1年時間,特別是在復雜病變,如主幹,分叉,鈣化,彎曲病變和急性心肌梗死,筆者也積累了一些經驗,隨訪的結果亦是安全和有效的。但應注意:ABSORB BVS支架骨架由聚L-乳酸組成,厚度達150um,1.通過病變較合金藥物支架困難,支撐力好的輸送系統和預擴張尤顯重要,特別是重度彎曲和鈣化病變,必要時加入extra-support wire或rotabladder;2.kiss-balloon技術不能運用於分叉中,分支的保護和順序擴張更顯重要;3.從IVUS或OCT檢查知道,植入BVS支架後的後擴張能使支架貼壁和遠期腔徑更佳;4.急性心肌梗死必須待血栓負荷完全消失後才能植入BVS支架。
當然,我們期待更多複雜冠脈病變中應用BVS支架的研究報導。
References:
[1]. Forrester, JS, et al., A paradigm for restenosis based on cell biology: clues for the development of new preventive therapies. J Am Coll Cardiol, 1991. 17(3): p. 758-69.
[2]. Oberhauser, JP, S. Hossainy and RJ Rapoza, Design principles and performance of bioresorbable polymeric vascular scaffolds. EuroIntervention, 2009. 5 Suppl F: p. F15-22.
[3]. Lobodzinski, SS, Bioabsorbable coronary stents. Cardiol J, 2008. 15(6): p. 569-71.
[4]. Yap, CH, et al., Does prior percutaneous coronary intervention adversely affect early and mid-term survival after coronary artery surgery? JACC Cardiovasc Interv, 2009. 2(8): p. 758-64.
[5]. Taggart, DP, Does prior PCI influence the clinical outcome of CABG? EuroIntervention, 2009. 5 Suppl D: p. D21-4.
[6]. Thielmann, M., et al., Prognostic significance of multiple previous percutaneous coronary interventions in patients undergoing elective coronary artery bypass surgery. Circulation, 2006. 114(1 Suppl): p. I441-7.
[7]. Koen Nieman., EA, Abstract 10570: ABSORB Cohort A Trial: Five Year Clinical and MSCT Results of the ABSORB Bioresorbable Everolimus Eluting Vascular Scaffold. 2011.
[8]. Serruys, PW, et al., A bioabsorbable everolimus-eluting coronary stent system (ABSORB): 2-year outcomes and results from multiple imaging methods. Lancet, 2009. 373(9667): p. 897-910.
[9]. Diletti, R., et al., 6-month clinical outcomes following implantation of the bioresorbable everolimus-eluting vascular scaffold in vessels smaller or larger than 2.5 mm. J Am Coll Cardiol, 2011. 58(3): p . 258-64.
[10]. Fernandez, D., et al., First experience of a bioresorbable vascular scaffold implantation in left main stenosis. Int J Cardiol, 2013.
[11]. Gogas, BD, et al., Three-dimensional reconstruction of the post-dilated ABSORB everolimus-eluting bioresorbable vascular scaffold in a true bifurcation lesion for flow restoration. JACC Cardiovasc Interv, 2011. 4(10): p. 1149-50.
[12]. van Geuns, RJ, et al., 3-Dimensional reconstruction of a bifurcation lesion with double wire after implantation of a second generation everolimus-eluting bioresorbable vascular scaffold. Int J Cardiol, 2011. 153(2): p. e43-5.






近期留言